Los Fertilizantes Fosfóricos para Maíz
Introducción
El material más utilizado para la elaboración de fertilizantes fosfóricos es la Roca Fosfórica (RF), donde el fósforo (P) se encuentra en forma de apatita Ca5(PO4)3(F,Cl,OH), mineral que proviene de depósitos ígneos y sedimentarios. Los minerales de depósitos ígneos regularmente presentan concentraciones bajas de P; en cambio las de origen sedimentario provienen de los depósitos insulares, correspondiendo a casi el 80 % de la producción total de RF. La RF presenta amplias variaciones en sus propiedades físicas y químicas: es un mineral poco reactivo y poco apto para aplicaciones directas a campo, pero puede ser sujeto de procesos físico-químicos para aumentar la concentración de P hasta alcanzar el 36 o 40 % de P2O5. Prácticamente toda la producción proveniente de estos depósitos es utilizada para la fabricación de fertilizantes (Fixen, 2009).
Fertilización fosfórica en maíz
El fósforo forma parte de las estructuras orgánicas, membranas celulares y ácidos nucleicos, es también el mayor participante en los compuestos energéticos que impulsan la fotosíntesis y el metabolismo de las plantas (Dood, 2005).
Investigaciones recientes han demostrado que para producir una tonelada de grano se requieren aproximadamente 9 kg de P2O5, del cual el 89 % al final del ciclo estará contenido en el grano. En relación a lo anterior, para una meta de rendimiento de 12 t/ha se requieren 108 kg de P2O5. Estudios realizados por la Universidad de Illinois encontraron que la máxima tasa de absorción de P2O5 fue de 2.4 kg/ha/día, consumiendo hasta antes de la fase fenológica R1, sólo el 46 % del fósforo demandado para la meta de rendimiento. Al final del ciclo la concentración de P en el grano fue de 3.3 g por kg cosechado (Bender, 2012).
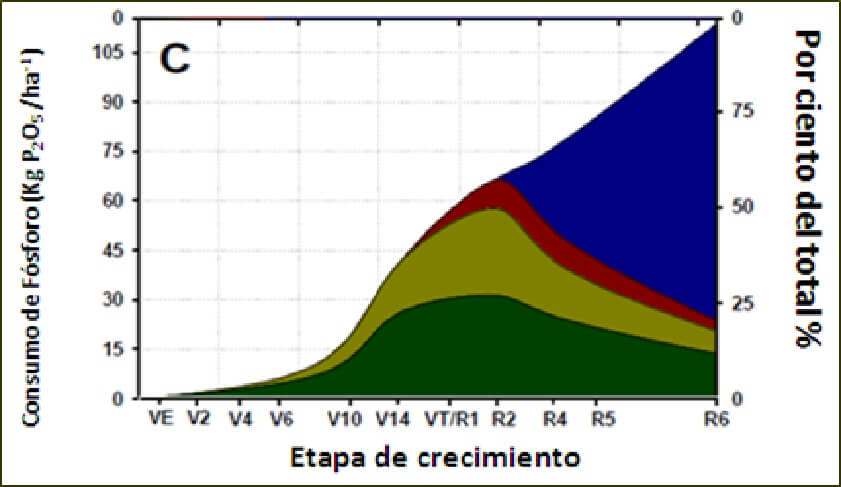
|
Figura 1. Acumulación de fósforo en Maíz para un rendimiento de 12 toneladas en Illinois en 2010. |
Consideraciones para la elección de fuentes apropiadas de fósforo
El pH del suelo es uno de los factores de mayor importancia en la elección de fuentes de fertilizantes de P. Así, el fosfato monoamónico (MAP) crea una zona más ácida alrededor de cada gránulo de fertilizante, mientras que el fosfato diamónico (DAP) crea una zona básica. Por lo tanto, en los suelos de pH alto, es preferible el uso de fertilizantes a base de MAP. El fertilizante de reacción ácida compensaría el ambiente básico que impera en los suelos calcáreos. Otro factor de importancia para la elección del fertilizante, es la toxicidad potencial del amoníaco en la germinación de semillas en suelos secos. La aplicación de la cantidad recomendada de P usando DAP contendrá aproximadamente un 60 % más de N que, en condiciones secas, ocasionaría una deshidratación de la semilla. Debe considerarse también la solubilidad de la fuente empleada, a diferencia de otros nutrientes de fácil lixiviación como el nitrógeno; el fósforo se mueve muy lentamente en el suelo, por tanto, la aplicación de este nutriente deberá realizarse antes de la siembra o al principio de ésta, en una sola exhibición, debido a que la difusión del fósforo en el suelo cuando está en forma de HPO4- es aproximadamente de 1 cm cada 3.1 años.
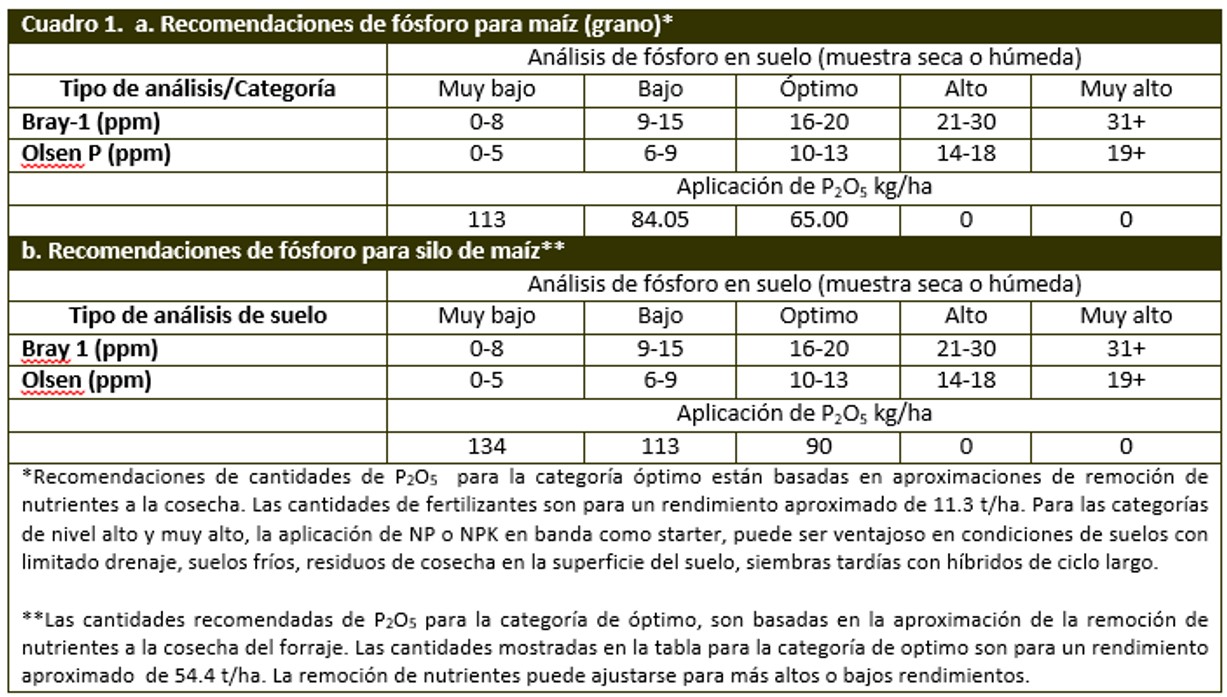
Recomendaciones de fertilización fosfórica a partir del contenido de P en el suelo según la Universidad de Iowa 2013
Fertilizantes fosfóricos comunes
Los términos con los que se expresan las cantidades de fósforo (P) son 2: fósforo disponible y fósforo soluble en agua. El termino P2O5 se deriva de la tendencia de expresar convenientemente las unidades fertilizante como equivalentes oxidados. Sin embargo el P no se encuentra como P2O5 en los abonos, solo es una expresión tradicional por el estado físico de los fertilizantes. (Lelkam, 2000).
El fósforo disponible expresado en P2O5 es el estimado del análisis de un material fertilizante. Normalmente una fracción de P disponible será soluble en agua. Por ejemplo 100 kg de un material con análisis (18-46-00), contiene 46 % de P2O5, de los cuales normalmente 95 % será soluble en agua. Por tanto, es importante recordar, que los fertilizantes son etiquetados con la cantidad disponible de P2O5. La mayoría de los productos fosfóricos que son vendidos, contienen el mayor porcentaje de P2O5 como soluble en agua.

|
Figura 2. Fertilizantes fosfóricos. De izquierda a derecha: Fosfato monoamónico, fosfato diamónico, superfosfato simple, súper fosfato triple y roca fosfórica. |
Fuentes de fertilizantes fosfóricos
Roca fosfórica: Su eficiencia en la disponibilidad del fósforo se estima en el laboratorio con ácido diluido (simulando la condición del suelo). Las fuentes clasificadas como altamente reactivas son más adecuadas para la aplicación directa en suelo. Se recomienda su uso en suelos ácidos. Generalmente con una disponibilidad de 30 a 33 % de P2O5.
Ácido fosfórico: Se obtiene principalmente por un proceso llamado “vía húmeda” que consiste en atacar la roca fosfórica con ácido sulfúrico. Las concentraciones de ácido fosfórico se expresan en porcentaje de P2O5. Comercialmente se encuentran concentraciones de 50 a 54 %.
Superfosfato simple: Fertilizante que ha disminuido su popularidad, se obtiene del tratamiento de RF con ácido sulfúrico y ácido cálcico, resultando fosfato mono cálcico con un contenido de 20 % de P2O5 y cerca de 12 % de sulfato, sus bajas concentraciones aumentan los costos de transportación.
Superfosfato triple: Llamado concentrado de superfosfato, resulta del tratamiento de rocas fosfóricas con ácido fosfórico, reduciéndose el contenido de S. Los contenidos de P2O5 oscilan entre 40 y 45 %. Es una buena fuente de P para el cultivo cuando no se requiere azufre.
Fosfato de amonio: Se origina de la reacción del ácido fosfórico y amoniaco anhidro. Contiene otros minerales mínimos como ácido sulfúrico y urea. De esta forma se obtienen 3 distintos fertilizantes.
Fosfato monoamónico (MAP): Producto obtenido de la reacción de NH3 con ácido sulfúrico. Los contenidos oscilan entre 12 % de N y 55 % de P2O5. Contiene impurezas pero no afectan su eficiencia, pudiéndose encontrar variantes comerciales con porcentajes crecientes de azufre (16-20-00-S15).
Fosfato diamónico (DAP): Se produce al reaccionar 2 moles de NH3 con un mol de ácido fosfórico. Es el fertilizante más comercializado en el mundo. Contiene regularmente 18-46-00. Su uso debe considerarse, debido a que altas tasas aplicadas en la siembra afectan la germinación al estar en contacto directo con la semilla por el proceso de ósmosis que se presenta en condiciones secas, además de la liberación de NH3, sobre todo en suelos con alto pH.
Polifosfatos de amonio (APP): Este material se forma cuando 2 moléculas de ácido fosfórico son combinadas químicamente por eliminación de agua. Posteriormente la cadena de fosfatos (poli fosfatos) es combinada con amoniaco y agua. Estos fertilizantes regularmente se encuentran en estado líquido con valores de 10-34-00. El porcentaje de fósforo disponible lo componen polifosfatos 60 % y el resto en forma de fosfatos normales.
Conclusión
Muchos fertilizantes fosfóricos se han desarrollado a partir de la roca fosfórica, sin embargo ésta por sí sola es poco reactiva y además poco homogénea, con baja concentración de fósforo. Una fuente ideal de P será aquella que sea económica de acuerdo a su contenido nutrimental soluble en agua y que sea conveniente usarla considerando su índice de acidez y su índice de salinidad. La aplicación de cualquier fuente de fertilizante está condicionada por el nivel de fósforo contenido en el suelo, la capacidad de fijar P de un suelo, y el pH del mismo.
Fuentes consultadas
D. F. Lelkam, W. N. S., E. J. Penas,. (2000). Phosphorus Sources for Corn Fertilization. National Corn Handbook. Retrieved from
Jason R. Dood, A. P. M. (2005). Soil-Test Phosphorus and Crop Grain Yiel Responses to Long-Term Phosphorus Fertilization for Corn- Soybean Rotations. Soil science society of America Journal, 69(Niveles de Respuesta fósforo), 1119-1128.
Paul E. Fixen. (2009). World fertilizer nutrient reserves. Paper presented at the Simposio de Fertilidad del Suelo 2009, Rosario, Argentina.
Roos Bender. (2012). NUTRIENT UPTAKE AND PARTITIONING IN HIGH-YIELDING CORN. Master of Science, University of Illinois at Urbana-Champaign,


